A Hepatite C e seu diagnóstico laboratorial
- Rosiane Ferrão
- 11 de jan. de 2019
- 9 min de leitura
SOBRE A DOENÇA
A Hepatite C é um importante problema de saúde pública. A doença é transmitida por contato direto com sangue de indivíduos infectados pelo Vírus da Hepatite C.
Estima-se que no mundo 71 milhões de indivíduos sejam portadores de Hepatite C crônica e que 400 mil vão a óbito em consequência da doença, principalmente devido à cirrose e carcinoma hepatocelular. A OMS, em parceria com a Organização Pan-Americana da Saúde (Opas) e o Center for Diseases Analysis (CDA) atualizou os dados para o Brasil, estimando que aproximadamente 0,7 % da população brasileira, entre 15 e 69 anos sejam sororreagentes (anti-HCV), sendo o total de aproximadamente 1.032.000 pessoas sororreagentes, e destes, 657.000 sejam virêmicos e que realmente necessitem de tratamento.
O período de incubação da doença é de 2 semanas a 6 meses, porém aproximadamente 80% dos casos são assintomáticos, o que dificulta o diagnóstico precoce.
Na infância a evolução da doença geralmente é benigna, com valores de enzimas hepáticas normais ou pouco elevadas e mínima atividade inflamatória ou fibrose. A resolução espontânea pode ocorrer em 25% a 40% dos lactentes, sendo menor em pré-escolares – cerca de 6% a 12% – e rara em crianças em idade escolar e na grande maioria dos casos a doença é assintomática.
Indivíduos infectados têm necessidades complexas e diversas e o conhecimento da prevalência da doença em determinada região pode levar as autoridades sanitárias locais à tomada de decisões ou estratégicas sanitárias que visem à diminuição de casos recentes e à melhoria dos cuidados com os indivíduos com doença instalada.
Em 1992 foi desenvolvido o primeiro teste para identificação do anticorpo contra o vírus da Hepatite C, e esta descoberta trouxe maior segurança nas transfusões sanguíneas. Em 1996 a doença foi incluída na Lista de Doenças de Notificação Compulsória do país.
A fase aguda da doença é pouco sintomática, o que leva, geralmente, à cronificação, daí a necessidade de um diagnóstico precoce.
A fase é considerada crônica quando atinge os 6 meses. A fase crônica também é muitas vezes assintomática, e esta infecção progressiva, ao longo da vida, pode levar à cirrose, insuficiência hepática e carcinoma hepatocelular.
O AGENTE ETIOLÓGICO
O vírus da Hepatite C pertence à família flaviridae, constituído por uma fita simples de RNA. Um vírus que tem grande tropismo pelo tecido hepático.
O vírus da Hepatite C só foi identificado em 1989, por Choo e col. Anteriormente era conhecida como Hepatite Não A Não B.
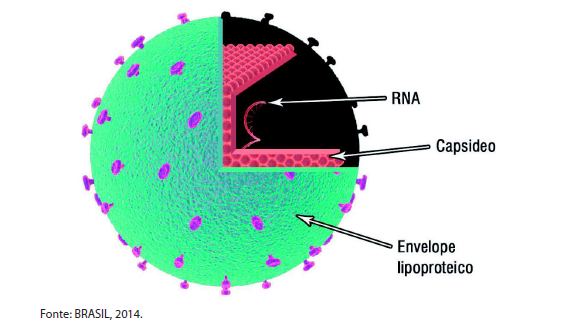
O vírus possui alta heterogeneidade genômica, devido às mutações que ocorrem em seu processo de replicação. Algumas regiões do vírus são altamente variáveis enquanto outras mais estáveis. Essas variações permitiram classificar o vírus em 7 grandes grupos ou genótipos, 67 subtipos identificados e 20 prováveis, e cerca de 100 diferentes cepas. No Brasil predomina o genótipo 1 sobre os demais, porém são encontrados com frequência os 1a, 1b, 2a, 2b e 3, sendo o genótipo 2 mais frequente na região centro-oeste e o genótipo 3 na região sul.
A taxa de replicação é bastante elevada, variando de 1010 a 1012 vírions por dia, na fase crônica da infecção.
TRANSMISSÃO
As principais vias de transmissão do vírus são a parenteral, por meio de compartilhamento de agulhas para uso de drogas injetáveis, reutilização ou falha de esterilização de equipamentos médicos e/ou odontológicos, falha de esterilização de equipamentos de manicure e o uso de hemoderivados contaminados. Pode ser, também, a via sexual, embora esta forma seja ineficiente e controversa, e a não adesão ao uso de preservativos é o fator que mais contribui para esta forma de transmissão.
A transmissão mãe/filho é rara, porém é a forma mais comum de infecção de recém-nascidos, e os principais fatores de risco são a viremia durante a gravidez e no momento do parto, e a coinfecção HCV e HIV.
A coexistência de outras doenças sexualmente transmissíveis, entre eles o HIV é um facilitador para a transmissão do HCV.
PATOGÊNESE
Devido à grande capacidade de mutação do vírus ele propicia um grande escape à resposta imunológica do indivíduo, o que leva a um alto índice de cronicidade (próximo a 80%). Essa constante mutação do vírus e suas múltiplas formas levam à um variado número de sequências genômicas virais, intimamente relacionadas, chamados de “quasispecies”, isto dificulta, até o momento, a produção de uma vacina.
A hepatite aguda tem difícil diagnóstico pelo fato de ser, em 84% dos casos, assintomática e por muitas vezes ser soronegativa, sendo identificada somente pela técnica de PCR. 20 a 30% dos casos apresentam-se com sintomas inespecíficos como anorexia, astenia, mal estar e dor abdominal, quadro clínico semelhante a outros quadros clínicos virais, e alguns indivíduos apresentam icterícia e escurecimento da urina.
Insuficiência hepática ou hepatite fulminante são bastante raros.
15 a 40% dos indivíduos infectados apresentam eliminação viral espontânea, e alguns fatores favorecem esta eliminação, como idade inferior a 40 anos, sexo feminino, aparecimento de icterícia e fatores genéticos como polimorfismo CC e interleucina 28B.
A hepatite se cronifica em 60 a 85% dos casos e, persistindo a viremia, 20% dos indivíduos desenvolvem cirrose após 10 a 30 anos, sendo esta evolução associada, entre outros fatores, a idade do indivíduo, consumo de álcool, coinfecção pelo vírus HIV ou HBV e o estado imunológico do indivíduo.
Indivíduos portadores de esquistossomose mansônica apresentam uma alteração na resposta imunológica gerando uma maior susceptibilidade à infecção pelo HCV. Esta coinfecção é uma das causas mais frequentes de descompensação hepatocelular. Estes indivíduos, ainda, apresentam aumento da persistência viral e a fibrose hepática desenvolve-se mais rapidamente.
A evolução crônica ocorre lentamente, com amplos aspectos clínicos, desde formas assintomáticas com enzimas normais, até hepatite crônica e hepatocarcinoma. A evolução fatal geralmente decorre de complicações como insuficiência hepatocelular, complicações referentes ao desenvolvimento de hipertensão portal – varizes esofágicas, hemorragia digestiva alta, ascite e encefalopatia hepática – além de trombocitopenia e desenvolvimento de carcinoma hepatocelular.
Algumas manifestações clínicas extra-hepáticas são comumente associadas à Hepatite C, sendo as mais comuns, a crioglobulinemia, glomerulonefrite, porfiria cutânea, Síndrome de Sjögren, tireoidite autoimune, líquen plano, linfoma de células B, fibrose pulmonar idiopática, poliartrite nodosa, anemia aplástica.
DIAGNÓSTICO
O diagnóstico da hepatite é feito, em grande parte dos casos, por acaso, através de resultados de exames de rotina já na fase crônica da doença.
O teste de triagem detecta anticorpos ou associação antígeno-anticorpo, sendo o anti-HCV o principal marcador. A sorologia não segue o padrão clássico de resposta IgM observada em outras infecções virais, pois pode estar ausente, tardia ou persistente após a infecção e pode não se relacionar com a atividade histológica.
Entre os testes moleculares têm-se os testes de detecção do ácido nucléico, que permitem detectar o RNA viral de todos os genótipos e subtipos de HCV. Estes testes podem ser quali ou quantitativos, e têm-se, também, os testes de genotipagem, que são baseados na amplificação do RNA viral, identificando os diversos genótipos, subtipos e populações mistas do HCV.
A triagem deve ser realizada por método que pesquise os anticorpos anti-HCV por metodologia sorológica clássica, ou utilizando o Teste rápido. O anti-HCV indica contato prévio com o vírus, não se podendo estabelecer se a infecção está ativa ou se foi resolvida. Por este motivo, para confirmação diagnóstica é utilizada a metodologia de biologia molecular. A realização de genotipagem depende da alternativa terapêutica a ser realizada.
Atualmente os testes de quimioluminescência têm se mostrado com excelente precisão e confiabilidade, maior especificidade, maior valor preditivo positivo e com sensibilidade semelhante aos EIA, e por este motivo estão sendo mais amplamente utilizados. Existem trabalhos, na literatura, que mostram a correlação entre os resultados positivos dos testes de triagem e os resultados do HCV-PCR (casos confirmados).

Fonte: J Clin Microbiol. Dec 2008;46(12): 3919-3923
São padronizados fluxogramas para a detecção do HCV. Veja:
1 - Investigação inicial da infecção pelo HCV usando testes rápidos para detecção do anti-HCV

Fonte: DIAHV/SVS/MS.
O Ministério da Saúde recomenda locais e situações em que os testes rápidos devem ser utilizados, e estas condições estão listadas a seguir:
*Serviços de saúde sem infraestrutura laboratorial ou localizados em regiões de difícil acesso;
*Instituições da Atenção Primária à Saúde (ex: UBS) e outras instituições pertencentes a Programas do Ministério da Saúde, tais como Rede Cegonha, Programa de Saúde da Família, Consultório na Rua, Quero Fazer, dentre outros programas;
*Centro de Testagem e Aconselhamento (CTA), Unidade de Testagem Móvel (UTM), Centro de Atenção Psicossocial (Caps), serviços de atendimento de emergência, pronto-socorro, hospitais e maternidades;
*Segmentos populacionais flutuantes;
*Populações vulneráveis:
**indivíduos com 40 anos de idade ou mais, indivíduos que realizaram transfusão, transplante, indivíduos em situação de compartilhamento de material de injeção.
**Comunicantes de pessoas vivendo com hepatites virais;
*Acidentes biológicos ocupacionais;
*Gestantes durante o pré-natal, parturientes e puérperas;
*Situação de abortamento espontâneo, independentemente da idade gestacional;
*Laboratórios que realizam pequenas rotinas (rotinas com até cinco amostras diárias para diagnóstico da infecção pela hepatite B ou C);
*Pessoas em situação de violência sexual;
*Outras situações especiais definidas pelo DIAHV para ações de vigilância, prevenção e controle das infecções sexualmente transmissíveis (IST), do HIV aids e das hepatites virais.
2 - Diagnóstico da infecção pelo vírus da hepatite C (HCV)
Neste fluxograma é utiliza um teste de triagem pela metodologia imunoensaio e um teste molecular, que detecta o RNA-HCV, como teste confirmatório:

Fonte: DAH/SVS/MS.
Caso a suspeita de infecção pelo HCV persista, sugere-se que uma nova amostra seja coletada 30 dias após a data da primeira amostra.
A repetição do teste molecular está indicada, a critério médico, nos seguintes casos: (1) suspeita de nova exposição nos seis meses que antecedem a realização da sorologia; (2) forte suspeita clínica de doença pelo HCV; (3) qualquer suspeita em relação ao manuseio ou armazenamento do material utilizado para realização do teste molecular. Além disso, o teste molecular deverá ser repetido nos casos de pacientes em diálise.
São definidas regras para a liberação dos laudos. Estas regras estão descritas no Manual Técnico Para Diagnóstico das Hepatites Virais, disponível em http://www.aids.gov.br/pt-br/pub/2015/manual-tecnico-para-o-diagnostico-das-hepatites-virais
O RNA viral pode ser detectado em aproximadamente 2 semanas após a infecção e o anticorpo anti-HCV em aproximadamente 30 a 60 dias após a infecção.
A Hepatite C aguda é definida através dos critérios:
1 -Soroconversão recente (há menos de seis meses) e com documentação de anti-HCV não reagente no início dos sintomas ou no momento da exposição, e anti-HCV reagente na segunda dosagem, realizada com intervalo de 90 dias; OU
2 - Anti-HCV não reagente e detecção do HCV-RNA em até 90 dias após o início dos sintomas ou a partir da data de exposição, quando esta for conhecida.
A Hepatite C crônica é definida através dos critérios:
1 -Anti-HCV reagente por mais de seis meses; E
2 - Confirmação diagnóstica com HCV-RNA detectável por mais de seis meses.
Vale lembrar que indivíduos imunossuprimidos e/ou em diálise, os indivíduos com infecção recente (menos de 30 dias, têm resposta inadequada ao teste anti-HCV, sendo necessária a realização dos testes de HCV-RNA.
Exames laboratoriais complementares recomendados aos indivíduos portadores de Hepatite C, na primeira consulta e durante o tratamento, lembrando que modificações podem ocorrer à critério do clínico, de sua conduta terapêutica.


O tratamento da Hepatite C é indicado para todos os pacientes infectados (infecção aguda ou crônica), independente do estadiamento da fibrose hepática, no entanto é fundamental o conhecimento desta, para se avaliar o esquema terapêutico a ser conduzido.
PREVENÇÃO
Como não há vacinas para a prevenção da Hepatite C, a prevenção depende da redução de riscos de exposição ao vírus. Deve se ter, então, atenção especial e não compartilhar agulhas, esterilizar equipamentos médicos, odontológicos e de manicure, análise completa do sangue para transfusões, uso de preservativos, higienização das mãos, não compartilhar de lâminas utilizadas para barbear ou depilar.
SIGLAS:

Por Rosiane e Silva Menezes Ferrão
*Farmacêutica-Bioquímica pela Universidade Federal de Minas Gerais (UFMG)
*Especialista em Análises Clínicas pela Universidade São Francisco (USF)
Bibliografia:
1 – FERREIRA, Walter A.; AVILA, Sandra L.M. Diagnóstico Laboratorial das Principais Doenças Infecciosas e Autoimunes. 2º ed., Rio de Janeiro: Guanabara Koogan, 2001. 443 p.
2 – PERONI, Carlos et al. Alta Prevalência do genótipo 1 em portadores de hepatite c Crônica em Belo Horizonte, MG. Revista da Sociedade Brasileira de Medicina Tropical. 41 (3):238-242, mai-jun,2008
3 – SCHUELTER-TREVISOL, Fabiana et al. Prevalência do vírus da Hepatite C entre contatos domésticos. Arq. Catarin. Med. 2012;41(2):09-14
4 – STRAUS, Edna. Hepatite C. Revista da Sociedade Brasileira de Medicina Tropical 34(1):69-82, jan-fev, 2001.
5 – JORGE, Stéfano Gonçalves. Hepcentro: Hepatologia Médica. 2007 Disponível em http://www.hepcentro.com.br/hepatite_c.htm. Acesso em: 05.jan.2019
6 – ARAUJO, Flávio Marcos Gomes. Variações nas regiões 5’ não traduzidas e na proteína não estrutural NS5A do vírus da Hepatite C em pacientes infectados com o genótipo 1. 2008. 138 p. Tese (Doutorado em Ciências da Saúde, Biologia Celular e Molecular) – Fundação Oswaldo Cruz, Centro de Pesquisas René Rachou, 2008.
7 - BRASIL. Ministério da Saúde. Manual Técnico para diagnóstico das Hepatites. Brasília: Secretaria de Vigilância em Saúde. Departamento de vigilância, prevenção e controle das IST, do HIV/AIDS e das Hepatites Virais. 2018
8 - BRASIL. Ministério da Saúde. Protocolo clínico e diretrizes terapêuticas para a Hepatite C e coinfecções. Brasília: Secretaria de Vigilância em Saúde.
Departamento de vigilância, prevenção e controle das IST, do HIV/AIDS e das Hepatites Virais 2018
9 - Ministério da Saúde. Secretaria de Vigilância em Saúde. Departamento de Vigilância, Prevenção e Controle das IST, do HIV/Aids e das Hepatites Virais. Telelab - Diagnóstico de Hepatites Virais. Brasília: Ministério da Saúde, 2014.
10– WORD HEALT ORGANIZATION (WHO). Hepatitis C –Disponível em https://www.who.int/hepatitis/es/ . Acesso em 06/01/2019.
11 – FOCCACIA, R et al. Estimated prevalence of viral hepatitis in the general population of the municipality of São Paulo, measured by serologic survey of a stratified, randomize and residence-basead population. Braz. Infec. Dis., 1998 Dec; 2(6):269-284.
12 – SILVA et al. Soroprevalência da Hepatite C em pacientes com esquistossomose. Revista Paranaense de Medicina, V.22 (1) jan a mar. 2008
13 – Sinyoung Kim, Jeong-Ho Kim, Seoyoung Yoon, Youn-Hee Park, and Hyon-Suk Kim. Clinical Performance Evaluation of Four Automated Chemiluminescence Immunoassays for Hepatitis C Virus Antibody Detection. JOURNAL OF CLINICAL MICROBIOLOGY, Dec. 2008, p. 3919–3923. Disponível em https://jcm.asm.org/content/jcm/46/12/3919.full.pdf Acesso em 10/01/2019






























Comentários